Acut myocardial infraction in young (< 50 y) patients: epidemiology and procedural features
█ Registry
DOI: 10.26430/CHUNGARICA.2019.49.4.255
Authors:
Baranyai Csaba1, Tóth Eszter Margi2, Márk László2, Jambrik Zoltán1
1Békés Megyei Központi Kórház, Invazív Kardiológiai Részleg, Gyula
2Békés Megyei Központi Kórház, Kardiológiai Osztály, Gyula
Summary
The cardiovascular disease shows a progressive nature. The acute myocardial infarction as a severe manifestation of a coronary heart disease usually occurs after 60 years of age. The aim of our study was to identify the risk profile and procedural features of patients with myocardial infarction younger than 50 years in our hospital.
Results: Overall 99 patients under 50y has been admitted to our hospital with myocardial infarction between Apr 2016 and Dec 2017. The mean age was 44±5,6 years, 72% of them was a male. A significant discrepancy between the risk profile know by the patients at the index event and the verified risk factors at admission was found (as hypertonia, hyperlipidaemia). A very high prehospital transit time till the hospital admission (976 min) was observed, what can be caused by the patients’ own delay. The need of prehospital reanimation was high in our young STEMI population (11.5%).
Summary: Myocardial infarction in younger than 50 years patients develops on a high cardiovascular risk basis and cardiac arrest frequently requires cardiopulmonary resuscitation.
ISSUE: CARDIOLOGIA HUNGARICA | 2019 | VOLUME 49, ISSUE 4
Összefoglalás
A kardiovaszkuláris megbetegedések progresszív jelleget mutatnak. Az akut miokardiális infarktus, mint a koszorúér-ateroszklerózis manifesztációja jellemzően 60 éves kor felett jelentkezik. Vizsgálatunk célja: beteganyagunkban az 50 év alatti betegek azonosítása, illetve adatainak feldolgozása.
Módszerek és betegek: A retrospektív adatgyűjtésben 2016 áprilisa és 2017 decembere közötti, a Békés Megyei Központi Kórház Invazív Kardiológiai Részlegén akut miokardiális infarktus miatt felvett és koszorúérfestésen átesett, 50 év alatti betegek kerültek a vizsgálatba. A betegek rizikófaktorait és procedurális adatait rögzítettük.
Eredmények: 99 esetben került 50 év alatti beteg miokardiális infarktus diagnózissal felvételre az adott időszakban. Átlagéletkoruk 44±5,6 év, 72% férfi. Mind a STEMI-, mind a NSTEMI-populációban jelentős eltérés mutatkozott a beteg által ismert, illetve valójában az esemény bekövetkeztekor fennálló főbb rizikófaktorok (hipertónia, hyperlipidaemia) között. STEMI esetén is jelentős volt a prehospitális késés (976 perc), amely nagyrészben a beteg hezitációjából állt. Magas volt a fiatal STEMI-s betegek esetén a prehospitális reanimáció szükségességének az aránya (11,5%).
Összefoglalásként elmondhatjuk, hogy az 50 éves kor alatt elszenvedett miokardiális infarktus magas kardiovaszkuláris kockázat talaján alakul ki és az átlagosnál gyakoribb reanimációs igény jelentkezik ellátása során.
Bevezetés
A kardiovaszkuláris megbetegedések körében az iszkémiás szívbetegség (ISZB) vagy koszorúér-betegség vezető halálok az európai és észak-amerikai országokban, incidenciája növekvő tendenciát mutat fiatal életkorban, amely korrelációt mutat a dohányzással, mozgásszegény életmóddal és fiatalkori obesitassal (1).
Az iszkémiás szívbetegség egyik akut manifesztációja a szívizominfarktus, amely általában az idősebb betegekben lép fel (átlagéletkor 65,7 év) (2).
A fiatalkori akut koronária szindróma (ACS) prevalenciája 6,3-12,8% közé tehető (1, 3). A legismertebb tanulmány, a Framingham Heart Study a fiatalkorban (55 év alatt) fellépő miokardiális infarktus 10 éves incidenciát férfiakban 51,1/1000-nek, míg nőkben 7,4/1000-nek állapította meg (4). Az utóbbi évtizedben azonban megfigyelték, hogy a fiatal STEMI-esetek incidenciája és mortalitása növekszik fiatal életkorú nőkben, de nem férfi sorstársaikban (5).
Kórházunkban végzett megfigyelés során Katona és munkatársai a 1970–1983 között, AMI miatt kezelt a 40 év alatti betegeknél úgy találták, hogy az összes infarktusban megbetegedettekhez viszonyítva a 40 év alattiak részesedése 4,04% volt (6).
Matsis és munkatársai vizsgálatában a fiatal populációban jellemzően a családi anamnézisben előforduló korai miokardiális infarktus, a dohányzás és az elhízás szerepelt vezető kardiovaszkuláris rizikófaktorként, míg a hipertónia, a hyperlipidaemia, a diabetes mellitus és a korábban elszenvedett miokardiális infarktus az idősebb betegekre volt jellemző. Shah és munkatársai 55 év alatti betegekkel végzett megfigyelése szerint a hyperlipidaemia szerepe kiemelt, a hipertónia pedig leggyakrabban kezeletlen magasvérnyomás-betegséget jelent. A dohányzás itt is jelentős faktorként szerepelt (1). Uhl és munkatársai leírásában százhatvanöt, 40 év alatti miokardiális infarktust elszenvedett beteg adatainak elemzése során csak 12%-ukban nem fordult elő a következő rizikófaktorok legalább egyike: elhízás, diabetes mellitus, hipertónia vagy hyperlipidaemia (7).
Célkitűzés
Retrospektív vizsgálatunkban célul tűztük ki az osztályunkon kezelt, miokardiális infarktuson átesett 50 év alatti betegpopuláció epidemiológiai jellemzőinek, esemény előtti kardiovaszkuláris státuszának, illetve a betegség klinikai lefolyásának megismerését.
Betegek és módszerek
Retrospektív vizsgálatunkban 2016 áprilisától–2017 decemberéig terjedő időszakban vizsgáltuk meg kórházunkban egymást követően akut miokardiális infarktussal kezelt 50 éves kor alatti betegek klinikai jellemzőit. Adatbázisunk kórlapok elemzéséből, a kórházi számítógépes adatbázisból lekért információkból, illetve a perkután koszorúér-intervenció (PCI) jegyzőkönyvéből került kitöltésre.
Kigyűjtésre kerültek többek között a beteg alapadatai (nem, születési év, kor, testsúly, testmagasság, majd ebből számítva a BMI – kg/m2 –, MI előtti kardiovaszkuláris rizikóstátuszuk meghatározása), a felvételét indokló diagnózis (STEMI/ NSTEMI). Az ellátásra vonatkozó alábbi adatok ugyancsak rendelkezésre állnak minden betegnél: prehospitális reanimáció szükségessége/részletei, a panasz kezdetétől az első orvosi ellátásig eltelt idő percekben (first medical contact, FMC), a panasz kezdetétől a koronarográfiáig eltelt idő percekben, mellkasi fájdalom megléte, beérkezési „high-sensitive” TroponinT-érték (TnT), 24 órás, kontroll TnT-érték, beérkezési kreatin-kináz (CK) és 24 órás, kontroll CK, EKG-eltérések (újonnan kialakult bal Tawara-szár-blokk, ST-eleváció, ST-depresszió), koronarográfia eredménye, perkután koronáriaintervenció (PCI) részletei (mely éren/ereken történt, beültetett stent adatai, egyéb a PCI során elvégzett jelentős kezelések, mint pl. a thrombusaspiráció, illetve glikoprotein IIb/IIIa adása. Az esemény előtti kardiovaszkuláris rizikó becsléséhez felmértük a beérkezéskor ismert hipertónia, hyperlipidaemia, dohányzás, diabetes mellitus, családi anamnézis pozitivitás, perifériás érbetegség, korábbi miokardiális infarktus/stroke, perkután vagy műtéti revaszkularizáció előfordulási arányát betegeinkben. Laborvizsgálatunk tartalmazta a beavatkozás utáni vesefunkciót, a gyulladásos állapotot, illetve a myocardiumnekrózis nagyságát leíró paramétereket. Echokardiográfia minden betegnél készült a beavatkozás után (24-48 órával), NSTEMI-vel érkező pácienseink esetén a beavatkozás előtt is. A prehospitális ellátást leíró adatok közül a direkt transzport arányát tartottuk mérvadónak. Az elbocsátáskor alkalmazott kezelés – acetilszalicilsav (ASA) clopidogrel/prasugrel/ticagrelol, béta-blokkoló, statin, angiotenzin-konvertáz enzim blokkoló (ACEI), protonpumpa-blokkoló (PPI) adása – részletesen regisztrálásra került.
A szívinfarktus diagnózisa minden esetben az érvényben lévő, 2018. évi ESC-ajánlás (8) szerint 3 pilléren (iszkémia vagy infarktus klinikai tünetei, iszkémiás EKG-eltérések, miokardiális károsodásra jellemző enzimemelkedés) alapult. Testtömegindexet (body mass index, BMI) a betegek testsúlyából és testmagasságából került kiszámításra: 30 feletti BMI esetén obesitasról, 25–30 közötti BMI-nél túlsúlyosságról beszélünk. Diabetes mellitusról akkor beszéltünk, ha az éhezési vércukorérték legalább két alkalommal ≥7,0 mmol/l vagy orális antidiabetikum szerepelt a rendszeres gyógyszerek között. Hyperlipidaemiaként (dyslipidaemiaként) értékeltük, az infarktus ellátása során vett laborban az teljes szérum koleszterinszint ≥5,2 mmol/l vagy teljes- és LDL-koleszterinszint emelkedésével HDL csökkenése társul vagy ha lipidcsökkentő terápia került beállításra korábban. Dohányzók közé került besorolásra, aki jelenleg aktív dohányzó vagy 6 hónapon belül szokott le a dohányzásról.
Hipertenziót azáltal állapítottuk meg, ha három különböző alkalommal a vérnyomás ≥140/90 Hgmm volt vagy antihipertenzív terápia került korábban beállításra. Kardiovaszkuláris anamnézis pozitivitásról akkor beszéltünk, ha a beteg kórtörténetében korábban elszenvedett iszkémiás szívbetegség (ISZB), agyi infarktus vagy perifériás artériás érbetegség (peripheral artery disease, PAD) szerepel. Pozitív családi anamnézist jelentette, ha a családban korábban koszorúér-esemény fordult elő (miokardiális infarktus, PCI, CABG-műtét).
Eredmények
Teljes infarktusos populáció alapadatai
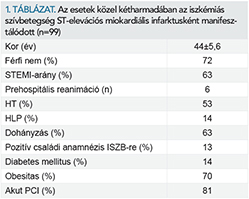
Az adott időszakban 99 alkalommal történt sürgős betegfelvétel szívkatéteres részlegünkre akut miokardiális infarktus iránydiagnózissal. Vizsgált populációnkban az átlagéletkor 44±5,6 év volt, a férfiak voltak többségben (72%) az irodalmi adatok alapján vártak szerint. Ahogyan az 1. táblázatban látható, az esetek közel 2/3-ában az iszkémiás szívbetegség ST-elevációs miokardiális infarktusként manifesztálódott. A betegcsoport kockázati faktorait elemezve azt láttuk, hogy a hipertónia és a hyperlipidaemia jelentősen kisebb számban volt ismert az esemény előtt, mint azok valós előfordulási aránya. Betegeink 53%-a tudott hipertónia betegségről, míg valójában 67%-ában volt jelen a betegség. Ugyanezek az arányok hyperlipidaemia esetén 14% és 64%.
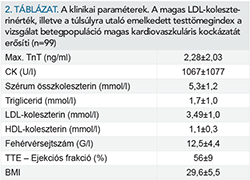
A 2. táblázatban klinikai paramétereket tüntettünk fel. A magas LDL-koleszterinérték, illetve a túlsúlyra utaló emelkedett testtömegindex a vizsgálat betegpopuláció magas kardiovaszkuláris kockázatát erősíti.
STEMI-populáció alapadatai
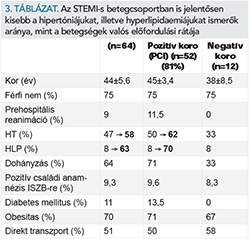
A férfiak dominanciája még kifejezettebb a STEMI-n átesett betegcsoportban, mint a NSTEMI-csoportban. STEMI iránydiagnózis esetén 81%-ban volt ateroszklerotikus eredet igazolható (1. típusú MI), míg a fennmaradó 19%-ban a koronarográfia nem talált okkluzív koszorúér-betegséget. Az STEMI-s betegcsoportban is jelentősen kisebb a hipertóniájukat, illetve hyperlipidaemiájukat ismerők aránya, mint a betegségek valós előfordulási rátája (3. táblázat: nyíl előtt a beérkezéskor a betegtől nyert adat, a nyíl mögött a vizsgálatokkal – vérnyomás-monitorizálás, laborvizsgálatok – igazolt, valóban fennálló hipertónia vagy hyperlipidaemia). Még kifejezettebb a magas kardiovaszkuláris kockázatú betegek aránya azoknál, akiknél katéteres metódussal bizonyított koszorúér-okklúzió áll a kórkép hátterében. Az „álpozitív” eseteknél (amikor ST-eleváció, mellkasi panasz miatt került a beteg sürgős felvételre, de a koronarográfia negatív lett) ugyanekkor alacsonyabb kardiovaszkuláris kockázati kép rajzolódik. Itt is feltűnő azonban a hipertónia magas előfordulási aránya. A negatív koronarográfiás eredményt adó betegeknél a STEMI diagnózis alapjául szolgáló EKG-felvételek áttekintése után is magas arányban (92%) találtunk ST-elevációt és/vagy ismeretlen ideje fennálló bal Tawara-szár-blokk morfológiát.
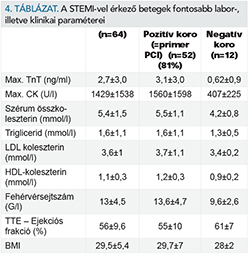
A STEMI-vel érkező betegek fontosabb labor-, illetve klinikai paramétereit a 4. táblázatban foglaltuk össze. Az echokardiográfiás vizsgálat minden betegnél a primer PCI után 24-48 órával készült.
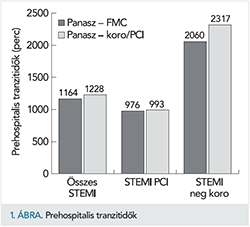
Időfaktor a STEMI-ellátás során
Az 1. ábra mutatja azt a jelentős prehospitális késést, amely a fiatal betegek ellátása során keletkezett. A magyar STEMI-ellátásra jellemző hosszú hezitációs időt is jelentősen meghaladó késés tapasztalható a panaszok fellépte és az első orvosi ellátás igénybevétele között.
NSTEMI-populáció alapadatai
35 beteg érkezett ezen időszakban NSTEMI iránydiagnózissal. Ezen esetekben minden betegnél több alkalommal pozitív magas szenzitivitású TnT szérumszintet mértünk és típusos mellkasi fájdalom együttes előfordulását figyeltük meg. A NSTEMI-vel érkező betegek invazív kardiológiai ellátása minden esetben 24 órán belül megtörtént. Kardiovaszkuláris rizikóprofiljukat az 5. táblázat mutatja.
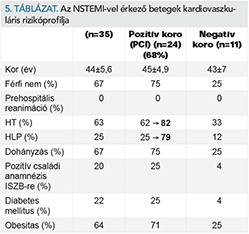
Azon betegnél, akinél 1-es típusú miokardiális infarktus zajlott, magas volt az ismert hipertóniások aránya. A hyperlipidaemia a betegek egynegyedénél volt ismert, kezelt. Ennek ellenére a valóságban mindkét betegség 80% körüli előfordulást mutatott, ami a dohányzással együtt igazolja a populáció magas kardiovaszkuláris kockázati statusát.
Reanimációval szövődött akut miokardiális infarktus 50 év alatt
Az adatok elemzése során kiemelendő a hirtelen halállal, illetve a következményes reanimációval szövődött infarktusok magas aránya. NSTEMI során a vizsgált, 50 év alatti populációban nem volt az infarktushoz kapcsolódó reanimáció. A primer katéteres intervención átesett, okkluzív koszorúér-betegséggel jelentkező betegek 11,5%-ában volt szükség a prehospitális szakban újraélesztésre (3. táblázat). Ez 5 esetben kamrafibrillációt jelentett, amelyet DC-sokk minden esetben sikeresen terminált. Egy esetben aszisztolé miatt folyamatos reanimáció során végeztük a katéteres revaszkularizációt.
Beavatkozás jellemzői STEMI esetén
STEMI-vel érkező betegeknél 52 esetben történt primer perkután intervenció. Koszorúerek közötti megoszlás: LAD 34, bal közös törzs 4, CX 11, RCA 19 esetben volt érintett. Harmickét betegnél a koszorúérfestés során az infarktust okozó ér teljes okklúziója volt igazolható. Tizenkilenc betegnél (36,5%) a magas thrombus telítettség miatt thrombusaspirációt végeztünk, 89%-ban pozitív eredménnyel.
A reanimált betegeknél 4 LAD, 1 bal közös törzs és 1 RCA intervencióra került sor, 2 esetben volt okkluzív a trombotikus lézió.
A betegek 32,6%-ában többér-betegséget mutatott.
Beavatkozás jellemzői NSTEMI esetén
NSTEMI esetén a koronarográfia 24 esetben volt pozitív, vagyis mutatott 50%-nál jelentősebb epikardiális koszorúér-átmérőcsökkenést. Egy betegnél diffúz, nonokkluzív koszorúér-érintettség miatt műtéti revaszkularizáció történt. Egy másik esetben az ismert CTO ellátása későbbi időpontban történt meg. Összesen 24 intervenciót végeztünk (egy betegnél két-ér PCI-re volt szükség): 11 LAD, 2 bal közös törzs, 7 CX, 9 RCA.
A betegek 33,3%-ában találtunk többér-betegséget, amely összevethető a STEMI-ben tapasztalt értékkel és alacsonyabb, mint az átlagos (idősebb) NSTEMI-populációban tapasztalténál.
Megbeszélés
A fiatalkori akut koronária szindróma (ACS) prevalenciája 6,3-12,8% közé tehető (1). A legismertebb tanulmány, a Framingham Heart Study, amely a fiatal miokardiális infarktust 55 év alatt definiálta, a 10 éves incidenciát férfiakban 51,1/1000-nek, míg nőkben 7,4/1000-nek állapította meg (4). Az utóbbi évtizedben azonban megfigyelték, hogy a fiatal STEMI-esetek incidenciája és mortalitása növekszik fiatal életkorú nőkben, de nem férfiak esetében (5).
Katona és munkatársai a 1970–1983 között végzett megfigyelése szerint a 40 éven aluliak aránya a miokardiális infarktust elszenvedett betegek között 4,04% volt. Infarktust megelőző mellkasi fájdalom mindössze 16%-ban volt jelen. Legjelentősebb kockázati tényezők a dohányzás (82%), a családi halmozódás (42%), a hypercholesterinaemia (18%) és a hipertónia (28%) voltak. A betegek fele említett az infarktust közvetlenül megelőző időintervallumban nagy fizikai terhelést (6).
Shah és társai 2016-ban megjelent vizsgálatai alapján 55 éves kor alattiak esetén többségében legalább egy tradicionális rizikófaktor biztosan fennállt. Összefoglalójuk szerint a hyperlipidaemia nagyon gyakran szerepelt rizikóként, de a hipertónia és a diabetes mellitus kiváltó szerepe kevésbé volt jelentős és az iszkémiás szívbetegség is ritkábban fordult elő fiatalkori miokardiális infarktusban (1). A dohányzás kiemelt rizikófaktornak számít, ugyanis 3,33-szoros rizikót jelent koronáriatörténés szempontjából. Oliveira és társai eredményei alapján azon 45 év alatti férfiak esetén, akik napi 15 szál cigarettánál többet dohányoztak 4,56-szoros rizikót jelentenek szívizominfarktus kialakulása szempontjából összehasonlítva a dohányzásról leszokottakkal. A fiatal populáció körében a férfi nem dominanciája kiemelendő jelentőségű (75-95% – 3,59 OR) (1, 9, 10), amelyet az is alátámaszt, hogy nem várt módon előrehaladottnak bizonyultak a koszorúerekben talált léziók 35 év alatti férfiak 20%-ában a boncolások szerint (11). Loughnan és munkatársai Melbourne-i vizsgálata 6 éves időintervallumra vonatkozott és eredményeik szerint a betegek 20%-a volt fiatalabb, mint 55 év (12).
Singh és munkatársai prospektív obszervációs vizsgálatában a fiatal STEMI-esetek klinikai jellemzőit, prevalenciáját és a fiatal akut szívinfarktus kimenetelét írták le a ≤45 évesek körében, megközelítőleg 1000 STEMI-beteg adatát dolgozták fel (1). A fiatal STEMI teljes prevalenciája vizsgálataik alapján 12,8%-ra (130 eset) volt tehető. Férfi dominancia volt jellemző (96,8%). Leggyakoribb rizikófaktorként a dohányzás (37,6%) volt felelőssé tehető, amelyet a diabetes mellitus (16,8%) és a hipertónia (16%) követett (13).
Matsis fiatalkorban főként a dohányzás és az elhízás szerepét látta jelentősnek, míg Uhl vizsgálatában az elhízáson, hyperlipidaemián és hipertónián kívül a diabetes mellitus megléte is jelentősnek bizonyult (7).
Az infarktushoz vezető rizikófaktorokat elemezve jelen vizsgálatunkban az esetek nagy részében fel nem ismert hipertónia és hyperlipidaemia, a dohányzás (teljes populációban 67-64-63%) és az elhízás (70%) mellett kiemelkedő előfordulást mutatott. Ez némi varianciát mutat a korábban közölt megfigyelésekkel (6).
Ugyancsak látható, hogy eredményeink illenek a nemzetközi irodalomban közölt megfigyelések sorába a fiatal betegek arányát illetően: kórházunkban az összpopulációhoz viszonyítva STEMI-s betegeink 12,4%-a, míg NSTEMI-s betegeink 7,1% 50 év alatti korosztályból kerül ki.
A fiatalkorban elszenvedett miokardiális infarktus esetén a férfi nem dominanciája általános az irodalomban, illetve nyomon követhető volt vizsgálatunkban is. Eredményeink alapján a fiatalkori szívinfarktus többsége ST-elevációval járó miokardiális infarktus, pontosan a vizsgált populáció 63%-a jelentkezett STEMI képében. A férfiak többsége (72%) volt kimutatható vizsgálatunkban, amelyet a korábban leírt irodalmi adatok is alátámasztanak, STEMI esetén 75%, míg NSTEMI esetében 67% volt a férfiak dominanciája. Oka valószínűleg a női nemet premenopauzálisan az ateroszklerózis progressziójával szemben védő női nemi hormon (ösztrogén) kardioprotektív szerepében kereshető (14), de itt meg kell jegyeznünk, hogy az utóbbi időben emelkedik a nők fiatal életkorban elszenvedett ST-elevációval járó miokardiális infarktusának esetszáma (5).
A fiatal betegek többségben az elülső falon alakult ki az infarktus (68,8%), amely az esetek felében egyér-betegségnek volt a következménye (50%) és a bal elülső leszálló artériában volt többnyire a culprit lézió (67,3%). Megközelítően normális vagy eltérés nélküli koronáriákat találtak az esetek 12,9%-ában (13). Vizsgálatunkban magas volt a STEMI esetén a többér-betegség aránya (32,6%), amely a populáció magas kardiovaszkuláris kockázatának eredménye. A bal elülső leszálló koszorúér domináns érintettsége vizsgálatunkban is kidomborodott STEMI és NSTEMI esetén egyaránt.
Talán a magasabb előfordulást mutató többér-betegség, illetve a LAD-érintettség miatt a prehospitális reanimáció aránya is különbözött az irodalomban közöltekétől. (A közelmúltban publikált vizsgálat szerint a prehospitális reanimáció 55%-a anterior érintettség esetén történt) (14). A reanimáció aránya 11,5% volt fiatal STEMI-s csoportunkban, amelynek valószínű oka az iszkémiás prekondicionálás hiánya lehet (15). Normál STEMI-populációban a prehispotális reanimáció előfordulási aránya 5-8%-ra tehető (16).
Vizsgálatunk korlátai
Természetesen tisztában vagyunk vizsgálatunk korlátaival és már körvonalazódtak is jövőben megvalósítandó terveink. Vizsgálatunk retrospektív adatgyűjtésen alapszik, amely korlátai mindenki által jól ismertek, ezért a jövőben prospektív vizsgálat indításán dolgozunk.
Kis esetszámú vizsgálatból (99 beteg) nem lehet messzemenő következtetéseket levonni a statisztikai próbák alkalmazásának limitáltsága miatt, ezért célunk a jövőben a mintavételi idő kiterjesztése 2013-tól és a folyamatosan gyarapodó adatállomány feldolgozása. A legnagyobb lehetőségek a többcentrumos adatfeldolgozásban rejlenének. Azt is figyelembe kell venni, hogy egyetlen régió ellátásának esetleges sajátosságai halmozottan jelenhetnek meg és eredményeinket szignifikánsan befolyásolhatják. Ezen kívül meg kell jegyeznünk, hogy csak a kórházi ellátásban részesülő fiatalkorú miokardiális infarktust elszenvedett betegek kerültek be a vizsgált populációba, a prehospitális ellátásban elhalálozott betegek nem kerültek feldolgozásra vizsgálatunkban.
Általános metodikai hibaforrás, hogy a szakirodalom sem egységes a fiatalkori MI-meghatározásnál. A fiatalkori miokardiális infarktussal foglalkozó vizsgálatokban változó az életkori meghatározás: általában ≤40–55 év alatti betegcsoportokat fogalmaztak meg fiatal miokardiális infarktusként, de nincs egyértelmű cut-off érték (9).
Következtetés
Mint azt a fent részletezett adataink alapján is láthatjuk a fiatalkorban fellépő miokardiális infarktus fokozott figyelmet és körültekintést érdemel, magas előfordulási aránya, illetve a hagyományos klinikumtól eltérő lefolyása miatt. Kiemelt hangsúlyt kell fektetni rizikócsoportok felkutatására, amelyet már tünet és panaszmentes betegeknél meg kellene kezdeni. Szembetűnő, hogy betegeink jelentős része számára fontos kardiovaszkuláris rizikófaktoraik nem voltak ismertek. A jövőben a férfi dominancia miatt talán meg lehet fontolni a <50–55 év alatti férfi korosztály rutinszerű szűrővizsgálatának bevezetését (hipertónia, lipidprofil, terheléses – főként képalkotó – vizsgálatok adott esetben) és a dohányzásról való leszokást támogató programok kiterjesztését. A kockázati faktorok felmérése után a közepes-magas kockázati betegeknél megfontolandó a koronária CT elvégzése (17). Talán a legtöbb potenciál a genetikai hajlam kimutatásában és ezáltal a génterápiában rejlik, amely alapjait már lefektették (18).
Irodalom
1. Shah N, et al. Myocardial Infarction in the “Young”: Risk Factors, Presentation, Management and Prognosis. Heart Lung Circ 2016; 25(10): 955–60. doi: https://doi.org/10.1016/j.hlc.2016.04.015
2. Fournier JA, et al. Myocardial infarction in men aged 40 years or less: a prospective clinical-angiographic study. Clin Cardiol 1996; 19(8): 631–6.
3. Matsis K, et al. Differing Clinical Characteristics Between Young and Older Patients Presenting with Myocardial Infarction. Heart, Lung and Circulation 2017; 26: 566–571. doi: https://doi.org/10.1016/j.hlc.2016.09.007
4. Avezum A, et al. Impact of age on management and outcome of acute coronary syndrome: observations from the Global Registry of Acute Coronary Events (GRACE). Am Heart J 2005; 149(1): 67–73.
5. Kannel WB, et al. Incidence and prognosis of unrecognized myocardial infarction. An update on the Framingham study. N Engl J Med 1984; 311(18): 1144–7.
6. Katona A, et al. Acut myocardiális infarktus 40 év alatti betegekben. Orv Hetil 1985; 126: 1161–1164.
7. Uhl GS, et al. Myocardial infarction in young adults: Risk factors and natural history. Am Heart J 1963; 105: 546–553.
8. Thygesen K, et al. Fourth universal definition of myocardial infarction. Eur Heart J 2019; 40(3): 237–269. doi: https://doi.org/10.1093/eurheartj/ehy462
9. Gebhard C, et al. Weather and risk of ST-elevation myocardial infarction revisited: Impact on young women. PLoS One 2018; 13(4): e0195602.
10. Oliveir A, et al. Tobacco smoking and acute myocardial infarction in young adults: a population-based case-control study. Prev Med 2007; 44(4): 311–6.
11. McGill HC, Jr. et al. Association of Coronary Heart Disease Risk Factors with microscopic qualities of coronary atherosclerosis in youth. Circulation 2000; 102(4): 374–9.
12. Loughnan ME, et al. Demographic, seasonal, and spatial differences in acute myocardial infarction admissions to hospital in Melbourne Australia. Int J Health Geogr 2008; 7: 42. doi: https://doi.org/10.1186/1476-072X-7-42
13. Singh B, et al. The prevalence, clinical spectrum and the long term outcome of ST-segment elevation myocardial infarction in young – A prospective observational study. Cardiovasc Revasc Med 2019; 20(5): 387–391. doi: https://doi.org/10.1016/j.carrev.2018.07.020
14. Karam N, et al. Incidence, Mortality, and Outcome-Predictors of Sudden Cardiac Arrest Complicating Myocardial Infarction Prior to Hospital Admission. Circ Cardiovasc Interv 2019. doi: https://doi.org/10.1161/CIRCINTERVENTIONS.118.007081
15. Murry CE, et al. Preconditioning with ischemia: a delay of lethal cell injury in ischemic myocardium. Circulation 1986; 74: 1124–1136.
16. Karam N, et al. Identifying Patients at Risk for Prehospital Sudden Cardiac Arrest at the Early Phase of Myocardial Infarction. Circulation 2016; 134(25): 2074–2083. doi: https://doi.org/10.1161/CIRCULATIONAHA.116.022954
17. Kolossváry M, et al. Comparison of Quantity of Coronary Atherosclerotic Plaques Detected by Computed Tomography Versus Angiograph. Am J Cardiol 2016; 117(12): 1863–7. doi: https://doi.org/10.1016/j.amjcard.2016.03.031
18. Cha K, et al. Genetic Variation at the ADAMTS7 Locus is Associated With Reduced Severity of Coronary Artery Disease. J Am Heart Assoc 2017. doi: https://doi.org/10.1161/JAHA.117.006928